Протон. Физика атома и атомного ядра. А все ли так на
самом деле?
ВСТУПЛЕНИЕ.
Представим читателю самому разобраться и дадим
один из классических примеров как
Ортодоксальная физика в учебниках превращает
желаемое в действительное.
«Представление об атомах как неделимых мельчайших частицах
вещества возникло еще в античные времена, но только в XVIII веке трудами
А. Лавуазье, М. В. Ломоносова и других ученых была доказана реальность
существования атомов. Но вопрос об их внутреннем устройстве даже не возникал, и
атомы по-прежнему считались неделимыми частицами. В XIX веке изучение
атомистического строения вещества существенно продвинулось вперед. В
1833 году при исследовании явления электролиза М. Фарадей установил,
что ток в растворе электролита это упорядоченное движение заряженных частиц –
ионов.
Фарадей определил минимальный заряд иона, который был
назван элементарным
электрическим зарядом. Приближенное значение которого оказалось равным e = 1,60·10–19 Кл.
На основании исследований Фарадея можно было сделать вывод
о существовании внутри атомов электрических зарядов.»
Смотрите сами, как нынче толкуется история всего столетней
давности. Оказывается, что Фарадей,
только введший понятие иона, определил его заряд на 58 лет раньше
действительной даты. Дж. Стони,1891 г. Это его Оригинальное название заряда
иона стало тогда «электрон». Фамилию
этого ученого сейчас почти не увидишь в
современной литературе…. А как
его звали даже в интернете можно найти с трудом…
http://www.bing.com/reference/semhtml/George_Johnstone_Stoney
Большую роль в развитии атомистической теории сыграл
выдающийся русский химик Д. И. Менделеев, разработавший в
1869 году периодическую систему элементов, в которой впервые был поставлен
вопрос о единой природе атомов.
Важным свидетельством сложной структуры атомов явились
спектроскопические исследования, которые привели к открытию линейчатых
спектров атомов. В начале XIX века были открыты дискретные
спектральные линии в излучении атомов водорода в видимой части спектра, и
впоследствии были установлены математические закономерности, связывающие длины
волн этих линий (И. Бальмер,
В 1896 году А. Беккерель обнаружил явление
испускания атомами невидимых проникающих излучений, названное радиоактивностью.
В последующие годы явление радиоактивности изучалось многими учеными
(М. Склодовская-Кюри, П. Кюри, Э. Резерфорд и др.). Было
обнаружено, что атомы радиоактивных веществ испускают три вида излучений
различной физической природы (альфа-, бета- и гамма-лучи). Альфа-лучи оказались
потоком ионов гелия. Бета-лучи – потоком электронов, а гамма-лучи – потоком
квантов жесткого рентгеновского излучения.
В 1897 году Дж. Томсон открыл электрон и измерил
отношение e / m заряда
электрона к массе. Опыты Томсона подтвердили вывод о том, что электроны входят
в состав атомов.
Но, в 1895 году Лоренц
уже сотворил свою силу, где использовался элементарный электрический заряд,
который был назван свободным…. И Только в 1900 году появилась теория
«свободных электронов» от Друде. Еще в
1895 году В опытах Можона было зарегистрировано отклонение уже !!!! частиц к отрицательному электроду
конденсатора в катодной трубке. Пусть сам читатель задумается…чих это рук
дело…. Введение электрона как частицы.
Но и автором была проведена кое-какая работа.
http://fatyf.aiq.ru/ELECTRON.htm
Таким образом, на основании всех известных к началу
XX века экспериментальных фактов можно было сделать вывод о том, что атомы
вещества имеют сложное внутреннее строение. Они представляют собой
электронейтральные системы, причем носителями отрицательного заряда атомов
являются легкие электроны, масса которых составляет лишь малую долю массы
атомов. Основная часть массы атомов связана с положительным зарядом.
9.1.
Опыт Резерфорда. Ядерная модель атома
Первая попытка создания модели атома на основе накопленных
экспериментальных данных принадлежит Дж. Томсону (
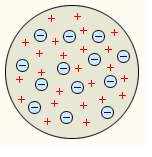
Модель атома Дж. Томсона.
Первые прямые эксперименты по исследованию внутренней
структуры атомов были выполнены Э. Резерфордом и его сотрудниками
Э. Марсденом и Х. Гейгером в 1909–1911 годах. Резерфорд предложил
применить зондирование атома с помощью α-частиц, которые возникают при
радиоактивном распаде радия и некоторых других элементов. Масса α-частиц
приблизительно в 7300 раз больше массы электрона, а положительный заряд равен
удвоенному элементарному заряду. В своих опытах Резерфорд использовал
α-частицы с кинетической энергией около 5 МэВ (скорость таких частиц
очень велика – порядка 107 м/с, но она все же значительно
меньше скорости света). α-частицы – это полностью ионизированные атомы
гелия. Они были открыты Резерфордом в 1899 году при изучении явления
радиоактивности. Этими частицами Резерфорд бомбардировал атомы тяжелых
элементов (золото, серебро, медь и др.). Электроны, входящие в состав атомов,
вследствие малой массы не могут заметно изменить траекторию α-частицы.
Рассеяние, то есть изменение направления движения α-частиц, может вызвать
только тяжелая положительно заряженная часть атома. Схема опыта Резерфорда
представлена на рис. 9.1.2.
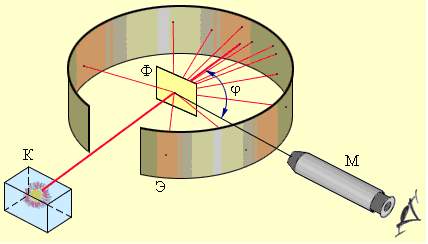
Схема опыта Резерфорда по рассеянию α-частиц. K –
свинцовый контейнер с радиоактивным веществом, Э – экран, покрытый сернистым
цинком, Ф – золотая фольга, M – микроскоп.
От радиоактивного источника, заключенного в свинцовый
контейнер, α-частицы направлялись на тонкую металлическую фольгу.
Рассеянные частицы попадали на экран, покрытый слоем кристаллов сульфида цинка,
способных светиться под ударами быстрых заряженных частиц. Сцинтилляции
(вспышки) на экране наблюдались глазом с помощью микроскопа. Наблюдения
рассеянных α-частиц в опыте Резерфорда можно было проводить под различными
углами φ к первоначальному направлению пучка. Было обнаружено, что
большинство α-частиц проходит через тонкий слой металла, практически не
испытывая отклонения. Однако небольшая часть частиц отклоняется на значительные
углы, превышающие 30°. Очень редкие α-частицы (приблизительно одна на
десять тысяч) испытывали отклонение на углы, близкие к 180°.
Этот результат был совершенно неожиданным даже для
Резерфорда. Он находился в резком противоречии с моделью атома Томсона,
согласно которой положительный заряд распределен по всему объему атома. При
таком распределении положительный заряд не может создать сильное электрическое
поле, способное отбросить α-частицы назад. Электрическое поле однородного
заряженного шара максимально на его поверхности и убывает до нуля по мере
приближения к центру шара. Если бы радиус шара, в котором сосредоточен весь
положительный заряд атома, уменьшился в n раз, то
максимальная сила отталкивания, действующая на α-частицу по закону
Кулона, возросла бы в n2 раз. Следовательно,
при достаточно большом значении n α-частицы могли бы
испытать рассеяние на большие углы вплоть до 180°. Эти соображения привели
Резерфорда к выводу, что атом почти пустой, и весь его положительный заряд
сосредоточен в малом объеме. Эту часть атома Резерфорд назвал атомным ядром. Так возникла ядерная
модель атома. Рис. 9.1.3 иллюстрирует рассеяние α-частицы в
атоме Томсона и в атоме Резерфорда.
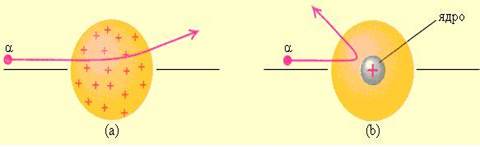
Рассеяние α-частицы в атоме Томсона (a) и в атоме
Резерфорда (b).
Таким образом, опыты Резерфорда и его сотрудников привели к
выводу, что в центре атома находится плотное положительно заряженное ядро,
диаметр которого не превышает 10–14–10–15 м. Это
ядро занимает только 10–12 часть полного объема атома, но содержит весь положительный заряд и не менее 99,95 % его массы.
Веществу, составляющему ядро атома, следовало приписать колоссальную плотность
порядка ρ ≈ 1015 г/см3. Заряд
ядра должен быть равен суммарному заряду всех электронов, входящих в состав
атома. Впоследствии удалось установить, что если заряд электрона принять за
единицу, то заряд ядра в точности равен номеру данного элемента в таблице
Менделеева.
Радикальные выводы о строении атома, следовавшие из опытов
Резерфорда, заставляли многих ученых сомневаться в их справедливости. Не
исключением был и сам Резерфорд, опубликовавший результаты своих исследований
только через два года (в
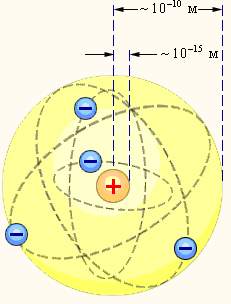
Планетарная модель атома Резерфорда. Показаны круговые
орбиты четырех электронов
«Планетарная модель атома, предложенная Резерфордом,
несомненно явилась крупным шагом в развитии знаний о строении атома. Она была
совершенно необходимой для объяснения опытов по рассеянию α-частиц. Однако
она оказалась неспособной объяснить сам факт длительного существования атома,
т. е. его устойчивость. По законам классической электродинамики, движущийся
с ускорением заряд должен излучать электромагнитные волны, уносящие энергию. За
короткое время (порядка 10–8 с) все электроны в атоме
Резерфорда должны растратить всю свою энергию и упасть на ядро. То, что этого
не происходит в устойчивых состояниях атома, показывает, что внутренние
процессы в атоме не подчиняются классическим законам.»
Комментарий.
Первое.
Модель атома
Резерфорда не является планетарной в чистом виде. Это потому что орбиты
электронов, якобы открытых Томсоном лежат не в плоскости вращения ядра. Не в
экваториальной плоскости. Если и существуют саттелиты у ядра, то их размер
должен быть хотя бы по порядкам быть близким к планетарным, как и в солнечной
системе, диаметр орбит и ядра тоже должен совпадать. И все это в силу просто
действия тех же сил, которые обеспечивают притяжение и планет к солнцу, т.е.
гравитации и электромагнитных сил.
Экваториальный
диаметр земли 2 6378.164 км 12756,328
км
Масса земли 5.976
1024 кг
масса Юпитера в массах земли 314.03= 1,876464
10 27 кг диаметр 142600000
м =1,426 10 5 м
Общая масса
планетной системы 448 масс Земли =2,677248 10 27кг
Диаметр системы в
плане 2. 5946 10 10 км
Диаметр солнца 2
6.9599 108 м 1,39198 10 9 м
Масса 1.989
Разница в массах
между наибольшей планетой и солнцем 3 – порядка
Разница в размерах
4 - порядка
|
0.8 . 10-13
|
см |
|
|
Масса
протона |
1.67 . 10-24
|
г |
Масса электрона в
1836 раз меньше массы протона 3-порядка
размер электрона
меньше, чем 10-
вроде бы все
нормально, но
для атома водорода
диаметр ядра 2х 0,53 10-
разница в 5
порядков между диаметром ядра и диаметром системы
а в солнечной
системе эта разница всего на один порядок
и даже для неона с
10 электронами порядок такой же.
Это говорит о
невозможности нахождения электронов на таких удаленных от ядра орбитах в силу
малости действия любых сил. Возникает сомнение в реальности существования таких
электронов в качестве саттелитов ядра атома. Еще сомнительно, что такие
электроны имеют одинаковую массу и размер.
Второе.
Превеликое сомнение в существовании
зарядовости ядра и спутников ядра – электронов. В принципе мы уже высказывались
о нереальности существования статического электричества (см.
http://fatyf.aiq.ru/electrostatics.htm
. Это дело и гораздо шире и глубже, и упирается в общую
электродинамику, в динамику излучений. То есть ни электроны и никакие другие
частицы не являются носителями электрических взаимодействий. Этим носителем
является свет в любых его проявлениях и различных энергий, это весь комплекс
электромагнитных излучений. Мало того исключительно волновая природа таких
излучений становится под сомнение, скорее потоковая, ближе к аэродинамике. Это
доказывает и поведение токов в плазме. А вот средой осуществляющей
взаимодействие является само вещество, и что возможно вездесущий эфир,
существование которого просто необходимо, если вещество отсутствует. И этим
эфиром необходимо считать само электромагнитное излучение… как
единственного реального кандидата на эту
роль.
Таким образом,
если и есть на самом деле электроны – спутники ядра, то их потенциал
относительно ядра не одинаков и не постоянен вследствие непрерывного обмена
энергией как внутри атомной системы, так и с окружающими атомами и он напрямую
связан как с массами составных частей системы, так и с размерами и диаметрами орбит.
В связи с этим необходимо отметить, что модели атома, основанные на
электростатической теории на все 100% ошибочны.
Более всего
напрашивается натуральная модель,
похожая на солнечную, с вращающимся ядром и вращающимися по стационарным
орбитам в плоскости экватора ядра спутниками различной массы и размеров. Данные
спутники не оказывают значительного влияния на энергетику системы атома в силу
малости размеров и массы, но достаточно сильно влияют на гироскопические
явления. Следует добавить, что открытие Томсоном электрона вещь сильно
натянутая и тоже не факт. (см. электрон).
Третье.
Если подойти более
корректно к опыту Резерфорда, то надо отметить, что альфа-излучение не есть
излучение ядер Гелия. Резерфорд специально помещал активный образец в колбу с
откачанным воздухом и обнаружил накопление гелия по истечении нескольких дней
опыта. Это не говорит об испускании ядер, но явно указывает на простое
образование гелия в результате распада атомов Радия и наличия действительно
неслабого по энергии излучения. К тому же было бы странно, что по пути своего
движения якобы ядра гелия не подхватывали бы якобы электроны прямо из
воздуха. Ведь Резерфорд проводил
представленный опыт по рассеянию именно на воздухе. Действительно, если
допустить, что это выделение гелия плюс излучение типа ультрафиолетового или
рентгеновского, то современными методами энергию этого излучения легко
определить. Результаты опыта легко
трактуются с точки зрения обычной оптики. Рассеяние объясняется по аналогии
с матовостью, обычное рассеяние видимого света на
полупрозрачных материалах. Здесь тоже свет, только невидимый.
Четвертое.
С точки зрения
химии модель с облаком отрицательно заряженных частиц вообще никуда не годится.
Электроны отталкиваются друг от друга. Молекула по идее тогда не должна иметь
места по причине отталкивания отрицательно заряженных оболочек атомов. И чем
электронов больше, тем сильнее должно
быть отталкивание. Но чтобы хоть как-то привязать электроны к атому придумали,
действительно, на основе химического многолетнего опыта, модель с орбиталями. И
на этой основе дотеоретизировались можно сказать до ручки. То есть уже не
проходит электростатическое отталкивание вообще. Появляется ковалентная связь –
пара электронов принадлежащая двум атомом. Один становится положительным ионом,
второй отрицательным. Имеем теперь электрический диполь. Совсем просто, если
наплевать на электростатику. А дальше еще полярная и неполярная ковалентная
связь со смещением заряда. Дипольный момент. И потом вспомнили электростатику,
появилась водородная связь, потом металлическая. В настоящее время всяческих
связей стало настолько много, что появились отдельные учебники по видам
химических связей. И все благодаря квантовой механике. Спасибо ей большое.
опыт Резерфорда по распаду радия
Предложение.
Следует принять
действительно планетарную модель атома. Или вообще от нее отказаться.
Необходимо отказаться от понятий электрона и протона как элементарных частиц.
Правда это нарушает почти столетие державшиеся убеждения о составе атома, но
зато дает возможность полностью пересмотреть современные теоретические основы
ядерной физики и признать их несостоятельность в силу огромного числа
нагромождений, ошибок и неправильных толкований результатов опытов.
Состав атомных ядер. Классика ядерной
физики.
К 20-м годам XX века физики уже не сомневались в том,
что атомные ядра, открытые Э. Резерфордом в
В настоящее время твердо установлено, что атомные
ядра различных элементов состоят из двух частиц – протонов
и нейтронов.
Первая из этих частиц представляет собой атом водорода, из
которого удален единственный электрон. Эта частица наблюдалась уже в опытах
Дж. Томсона (
Опять Томсон и опять частица…. Томсон в то время определял массы на им же
изобретенном масс спектрометре, заполняя катодную трубку различными газами и
определяя степень смещения катодного луча. При этом тем же Томсоном в 1897 году
было заявлено, что катодные лучи не отклоняются в присутствии разреженных
газов. Такой трактовке работ Томсона грош цена, поскольку заранее знать заряда
частицы он не мог. Не иначе использовался уже известным способом полученный
заряд электрона.
В 1919 году
Э. Резерфорд обнаружил ядра атома водорода в продуктах расщепления ядер
атомов многих элементов. Резерфорд назвал эту частицу протоном. Он высказал
предположение, что протоны входят в состав всех атомных ядер. Схема опытов
Резерфорда представлена на рис. 9.5.1.
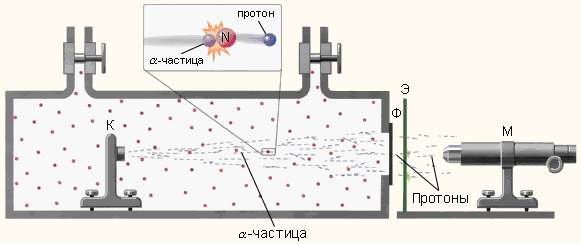
Схема опытов Резерфорда по обнаружению протонов в продуктах
расщепления ядер. К – свинцовый контейнер с радиоактивным источником
α-частиц, Ф – металлическая фольга, Э – экран, покрытый сульфидом цинка, М
– микроскоп.
Прибор Резерфорда состоял из вакуумированной камеры, в
которой был расположен контейнер К с источником α-частиц. Окно камеры было
закрыто металлической фольгой Ф, толщина которой была подобрана так, чтобы
α-частицы не могли через нее проникнуть. За окном располагался экран Э,
покрытый сернистым цинком. С помощью микроскопа М можно было наблюдать
сцинтилляции в точках попадания на экран тяжелых заряженных частиц. При
заполнении камеры азотом при низком давлении на экране возникали световые
вспышки, указывающие на появление потока каких-то частиц, способных проникать
через фольгу Ф, практически полностью задерживающую поток α-частиц.
Отодвигая экран Э от окна камеры, Резерфорд измерил среднюю
длину свободного пробега наблюдаемых частиц в воздухе. Она оказалась
приблизительно равной
По современным измерениям, положительный заряд протона в
точности равен элементарному
заряду e = 1,60217733·10–19 Кл,
то есть равен по модулю отрицательному заряду электрона. В настоящее время
равенство зарядов протона и электрона проверено с точностью 10–22.
Такое совпадение зарядов двух непохожих друг на друга частиц вызывает удивление
и остается одной из фундаментальных загадок современной физики. Масса протона, по современным измерениям, равна mp = 1,67262·10–27 кг. В
ядерной физике массу частицы часто выражают в атомных единицах массы
(а. е. м.), равной ![]() массы атома
углерода с массовым числом 12:
массы атома
углерода с массовым числом 12:
1 а. е. м. = 1,66057·10–27 кг.
Следовательно, mp = 1,007276 · а. е. м.
Во многих случаях массу частицы удобно выражать в эквивалентных значениях
энергии в соответствии с формулой E = mc2. Так как
1 эВ = 1,60218·10–19 Дж, в энергетических
единицах масса протона равна 938,272331 МэВ.
Таким образом, в опыте Резерфорда было открыто явление
расщепления ядер азота и других элементов при ударах быстрых α-частиц и
показано, что протоны входят в состав ядер атомов.
После открытия протона было высказано предположение, что ядра
атомов состоят из одних протонов. Однако это предположение оказалось
несостоятельным, так как отношение заряда ядра к его массе не остается
постоянным для разных ядер, как это было бы, если бы в состав ядер входили одни
протоны. Для более тяжелых ядер это отношение оказывается меньше, чем для
легких, т. е. при переходе к более тяжелым ядрам масса ядра растет
быстрее, чем заряд.
Замечания к опыту.
Самое простое,
столкновение упругое и тогда невозможно появление частицы, столкновение
не упругое, тогда разрушение атома азота.
В те времена
Азот в камере
совпадение спектральных линий азота и самого излучения а так же и
спектров регистрирующего покрытия.
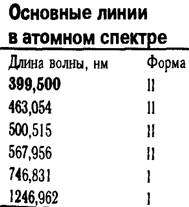 азот
азот 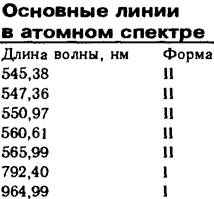 сера
сера цинк
цинк
Близость спектров в видимой области очевидна
для газового состояния атомов азота и находящихся в неравных условиях (твердое
состояние) атомов молекул сернистого цинка. То есть необходимо учитывать и
изменчивость спектров у твердых тел по сравнению с газообразным состоянием.
Только так можно объяснить различие в
проникающей способности
Достаточно хорошо известно, что
альфа-частицы, как принято, уже и спорить вроде
даже стыдно как –то, НО ПОСПОРИМ ЕЩЕ РАЗ, якобы ядра гелия имеют
очень малую проникающую способность.
Длина пробега таких частиц в воздухе
составляет сантиметры. А посему в данном случае вопрос, какой был вакуум.
Почему не произведен сравнительный анализ количества сцинциляций при разных
давлениях. Каким образом частицы не пролетающие больших расстояний в воздухе,
минуют сравнительно толстую фольгу в окошке и уже в воздухе вызывают свечение
экрана.
При
заполнении баллона азотом эта длина тоже невелика. То есть альфа-частицы в
принципе не смогут достигнуть металлической фольги, а тем более проникнуть
сквозь нее. Теперь о вышибании протонов. А кто проверял после этого эксперимента
процент оставшегося азота. Должна несомненно произойти, и без всякого
ускорителя ядерная реакция следующего типа:
2р2n- + N(Z=7,M=14)--> неизвестно что+ протон?
Протон то улетел. А и Б сидели на трубе, А упало, Б пропало, что осталось на трубе ???
И это главный минус этого опыта. В противном
случае если анализ покажет отсутствие каких либо новых атомов, то следует
предположить:
А вот жесткое излучение может. А ля
телевизионная труба, только вместо катода,
радиоактивный образец. И что интересно результат опыта будет совершенно одинаков!
Вообще, каким образом протон проникнет сквозь
фольгу, опять не рассеиваясь.
О
каких протонах вообще может идти речь? A? !!!!!!!!!!!
О Каких электронах разговор?
Самый главный аргумент в пользу излучения, то
есть света (ультрафиолет, рентген, гамма излучение) это их преобладание
количественное – излучений больше, над электронным током. А то какой-то сумбур
– то излучение, то электроны, то опять излучение. То фотоны, то электроны.
Делаем просто = это все излучение и никаких
вам электронов в принципе. Просто излучение разных частот-энергий!!!!!!!
Фатьянов А.В. 2009